Te grondig zoeken naar contrastnefropathie
1 reactieVeiligheidsprogramma overschat het aantal risicopatiënten
Er vindt veel radiologisch onderzoek plaats waarbij jodiumhoudende contrastmiddelen worden gebruikt. Voor patiënten met een verhoogd risico op contrastnefropathie zijn preventieve maatregelen nodig. Maar wanneer is iemand een hoogrisicopatiënt?
Uit onderzoek naar vermijdbare, onbedoelde schade en sterfte in Nederlandse ziekenhuizen, dat het Nivel in opdracht van de Orde van Medisch Specialisten in 2007 heeft verricht, kwamen tien als ‘hoog vermijdbaar’ geclassificeerde schades naar voren. Deze vormen de pijlers van het VMS-programma (veiligheidsmanagementsysteem).2 Doelstelling van dit programma is de vermijdbare schade te halveren. Hiertoe moeten ziekenhuizen maatregelen nemen en registraties invoeren.
Eén van de tien onderdelen van het VMS-programma is het voorkómen van contrastnefropathie bij patiënten die radiologisch onderzoek met jodiumhoudende contrastmiddelen ondergaan. Dat kan door het identificeren van alle patiënten met een verhoogd risico op contrastnefropathie en het nemen van adequate preventieve maatregelen bij hoogrisicopatiënten.3 Dit specifieke programma is gebaseerd op de CBO-richtlijn ‘Voorzorgsmaatregelen bij jodiumhoudende contrastmiddelen’ uit 2007.4 Daarmee lijkt dit VMS-programma evidence-based. Maar is dat ook zo?
Contrastnefropathie
Contrastnefropathie wordt gedefinieerd als een stijging in het serum creatinine van 44 µmol/l of van 25 procent binnen twee tot drie dagen na toediening van het contrastmiddel. Meestal is deze verslechtering van de nierfunctie tijdelijk, en slechts zelden leidt dit tot blijvend nierfunctieverlies of (tijdelijke) noodzaak tot een nierfunctievervangende behandeling. Contrastnefropathie is in observationeel onderzoek geassocieerd met een verhoogd risico op complicaties, verlengde duur van ziekenhuisopnames en overlijden.5 Vanwege deze ‘harde’ eindpunten, waaronder blijvend nierfunctieverlies, is het belangrijk om contrastnefropathie te voorkomen. Of de ‘harde’ langetermijneindpunten causaal gerelateerd zijn aan het optreden van de tijdelijke nierfunctieverslechtering, is overigens niet duidelijk. Waarschijnlijk ontwikkelen vooral ziekere patiënten contrastnefropathie en hangt de verhoogde kans op complicaties en sterfte ook samen met de onderliggende ziekte.
Hoogrisicopatiënten
De prevalentie van contrastnefropathie hangt sterk af van risicofactoren bij de onderzoekspopulatie – een gestoorde nierfunctie is de belangrijkste – en kan oplopen tot 50 procent. In het VMS-programma worden hoogrisicopatiënten gedefinieerd als patiënten met een eGFR (nierfunctie) van minder dan 45 ml/min/1,73m2, of een eGFR van minder dan 60 ml/min/1,73m2 bij patiënten met diabetes mellitus of met twee of meer risicofactoren.
Waarschijnlijk ontwikkelen vooral ziekere
patiënten contrastnefropathie
In Nederland worden jaarlijks een half tot één miljoen onderzoeken verricht waarbij intravasculair jodiumhoudende contrastmiddelen worden toegediend. Hoeveel van deze onderzoeken plaatsvinden bij hoogrisicopatiënten is opmerkelijk genoeg niet bekend. Op grond van kleinschalig onderzoek door degenen die het VMS-programma hebben ontwikkeld, schat men dat het om 10 tot 15 procent van de poliklinische patiënten gaat en tot 30 procent van de klinische patiënten. Dit betekent dat er per jaar 100.000 tot 150.000 onderzoeken met intravasculair contrast worden uitgevoerd bij hoogrisicopatiënten.
Preventieve maatregelen
Het VMS-programma beveelt bij de hoogrisicopatiënt naast algemene maatregelen, zoals het tijdelijk staken van diuretica en NSAID’s, een aantal specifieke maatregelen aan, zoals: medicatieadvies (bijvoorbeeld tijdelijk staken van metformine, vanwege mogelijk nierfunctieverlies), beperking van de dosis jodiumhoudend contrastmiddel en hydratie.3
De basis voor preventie in het VMS-programma is zorgen voor een goede hydratietoestand voorafgaand aan het contrastonderzoek. Hydratie bij hoogrisicopatiënten gebeurt door intraveneuze toediening van natriumchloride (0,9%) gedurende vier uur voor en vier uur na het contrastonderzoek. Hiervoor is een dagopname noodzakelijk. Bij patiënten met hartfalen of een ernstig gestoorde nierfunctie moet natriumchloride in een lang schema worden toegediend, waarvoor een klinische opname noodzakelijk is. In acute situaties kan worden gehydreerd met natriumbicarbonaat 1,4 procent 3 ml/kg in één uur voor de ingreep en 1 ml/kg/uur gedurende zes uur na de ingreep. Aanvankelijk werd gedacht dat bicarbonaat effectiever zou zijn dan hydratie door natriumchloride-infusie, maar recente meta-analyses tonen aan dat dit niet vaststaat.6 7 Hydratie door bicarbonaatinfusie is gelijkwaardig aan hydratie door natriumchloride-infusie.6 7 De cruciale vraag is vervolgens hoe effectief hydratie met natriumchloride eigenlijk is.
Hydratie
De reden voor hydratieschema’s met natriumchloride is dat in epidemiologisch onderzoek contrastnefropathie vaker voorkomt bij gedehydreerde patiënten en dat hydratie in dierexperimenten de incidentie van contrastnefropathie verlaagt. Opmerkelijk genoeg is er slechts één gerandomiseerd ‘placebo’-gecontroleerd onderzoek verricht naar het effect van hydratie met natriumchloride bij patiënten.8 Dit is een kleinschalig onderzoek bij 53 patiënten die een hartkatheterisatie ondergingen, waarbij de meesten niet tot de gedefinieerde hoogrisicogroep behoorden. Dit onderzoek liet een opmerkelijk gunstig effect zien van natriumchloride op de nierfunctie. Dit is slechts een surrogaatuitkomstmaat, met een voorspelbaar effect op het onderzochte eindpunt. Door de (over)hydratie zal immers ook het serum creatinine dalen. Ondersteunend bewijs voor de effectiviteit van hydratie is nog de studie van Chen c.s.9 In de subgroep van patiënten met een creatinine hoger dan 130 µ/l (gemiddeld 221 µ/l) werd een effect van hydratie gevonden op de incidentie van contrastnefropathie.
Hydratie gebeurde in deze studie echter met natriumchloride 0,45 procent (in combinatie met acetylcysteïne), en niet met natriumchloride 0,9 procent zoals het VMS-programma adviseert.
Voor de kliniek zijn bovendien andere eindpunten belangrijk, namelijk de incidentie van blijvend nierfunctieverlies, de duur van de ziekenhuisopname en de kans op complicaties en overlijden. Opmerkelijk genoeg is er geen gerandomiseerd onderzoek naar de effectiviteit van hydratieschema’s op deze relevante uitkomstmaten. Het hydratieadvies is dus niet evidence-based. Het berust vooral op expert opinions gebaseerd op dierexperimenteel en epidemiologisch onderzoek en op klinische ervaring.
Poliklinieken
Vanwege het VMS-programma moet voorafgaand aan jodiumhoudend contrastonderzoek van iedere patiënt worden beoordeeld of hij tot de hoogrisicogroep behoort.4 Daartoe moet van elke patiënt de nierfunctie bekend zijn of worden gemeten. Bij een eGFR lager dan 60 ml/min/1,73m2 moet worden bekeken of er andere risicofactoren zijn.4 Om dit proces te operationaliseren openen veel ziekenhuizen zogeheten contrastnefropathiepoli’s, waar een internist of een nurse practitioner de patiënten ziet. Hoogrisicopatiënten krijgen daar medicatieadviezen en er wordt een (dag)opname geregeld voor hydratie. De logistieke consequenties van de noodzaak tot poliklinische consulten, opnames voor hydratie en planning van contrastonderzoeken zijn dus groot. Omdat het om veel patiënten gaat, is een forse inspanning van ziekenhuispersoneel en veel geld nodig.
Verplichte indicator
Naast deze logistieke consequenties zijn er ook administratieve gevolgen. Ziekenhuizen moeten registraties invoeren en procesindicatoren bijhouden. Bekend moet zijn bij welk percentage van de patiënten de nierfunctie bekend is voor contrasttoediening, en bij welk percentage van de hoogrisicopatiënten er inderdaad hydratie heeft plaatsgevonden. Aanvankelijk gebeurt dit vrijwillig, maar te zijner tijd zal dit een verplichte kwaliteitsindicator worden waarop de Inspectie voor de Gezondheidszorg ziekenhuizen beoordeelt. Het VMS-programma heeft dus verstrekkende gevolgen.
Het VMS-programma beoogt vermijdbare schade te beperken, maar er kunnen ook nadelige neveneffecten aan kleven. Zo wordt er een beeld gecreëerd dat intraveneus jodiumhoudend contrastonderzoek schadelijk is. De ervaring leert dat de vrees voor contrastnefropathie bij patiënten en aanvragers kan leiden tot het uitstellen of zelfs vermijden van medisch geïndiceerd contrastonderzoek, wat nadelige effecten kan hebben.
Voorstel tot verandering
Het VMS-programma preventie contrastnefropathie is inmiddels in diverse ziekenhuizen ingevoerd en wordt in de overige ziekenhuizen voorbereid. De praktische consequenties ervan worden nu in volle omvang zichtbaar. We kunnen nu dus de voor- en nadelen onder de loep nemen. Daar de effectiviteit van het programma op relevante uitkomstmaten onbekend is, de last voor patiënten en de gezondheidszorg groot is, en de kans bestaat dat er onbedoelde nadelige effecten optreden, pleiten wij ervoor om het programma aan te passen. Tijdens de Nederlandse Nefrologiedagen is hierover gedebatteerd. Na afloop vond ongeveer driekwart van de aanwezigen dat het programma zou moeten worden aangepast.
Het is beter om de definitie van hoogrisicopatiënten
aan te passen
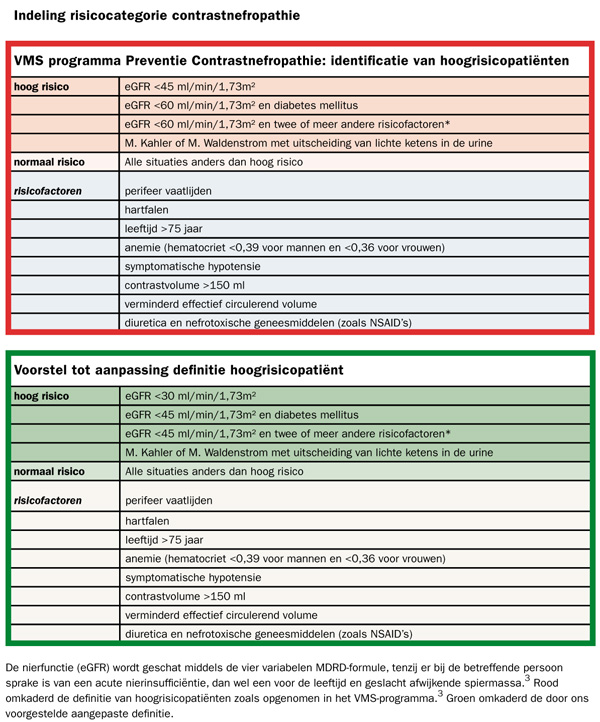
Wij stellen voor de definitie van hoogrisicopatiënten aan te passen. In plaats van eGFR-waarden van 45 en 60 ml/min/1,73m2 (tabel) kunnen eGFR’s van 30 en 45 ml/min/1,73m2 worden gehanteerd. Dat maakt de groep hoogrisicopatiënten aanzienlijk kleiner. Het VMS-programma wordt zo werkbaar en de kosten nemen aanzienlijk af.
Dat er geen wetenschappelijk bewijs is voor deze aanpassing, is geen argument, aangezien er ook geen wetenschappelijk bewijs is voor het nu in te voeren programma. Bij de patiënten die door ons voorstel worden uitgesloten, zou in een prospectief cohortonderzoek het risico op contrastnefropathie, maar met name het risico op relevante uitkomstmaten moeten worden bekeken. Of in een gerandomiseerd onderzoek met voldoende power zou de effectiviteit van een preventief programma op relevante uitkomstmaten kunnen worden onderzocht. Dergelijke analyses kunnen leiden tot een evidence-based VMS-programma preventie contrastnefropathie.
Onbedoelde effecten
De aandacht op het voorkómen van contrastnefropathie is nuttig en belangrijk. De groep hoogrisicopatiënten die door het huidige VMS-programma wordt vastgesteld, is echter te omvangrijk. De effectiviteit van de preventieve maatregelen om relevante eindpunten te voorkomen, is bovendien onbekend, evenals de kosten van dit programma. Tot slot bestaat de kans dat het programma tot onbedoelde nadelige effecten leidt. Daarom roepen wij de expertgroep die het VMS-programma preventie contrastnefropathie begeleidt op om het programma aan te passen.
dr. R.T. Gansevoort,1
dr. C.A.J.M. Gaillard,
dr. M.H. Hemmelder,
dr. Y.W.J. Sijpkens,
allen internist-nefroloog
Correspondentieadres: r.t.gansevoort@int.umcg.nl; c.c.: redactie@medischcontact.nl.
Geen belangenverstrengeling gemeld.
Samenvatting
- Recentelijk is het VMS-programma ‘voorkomen van contrastnefropathie bij patiënten die radiologisch onderzoek met jodiumhoudende contrastmiddelen ondergaan’ ingevoerd.
- De doelstelling van dit programma wordt door ons onderschreven.
- We willen de bewezen effectiviteit van het programma op relevante uitkomstmaten in relatie tot de lasten voor patiënten en de gezondheidszorg echter nuanceren.
- Deze nuancering resulteert in een oproep om het programma aan te passen.
Referenties
1. Dit betoog wordt ook onderschreven door: dr. M. van Buren, internist-nefroloog, prof. dr. R.O.B. Gans, internist, dr. C. Hagen, internist-nefroloog, en prof. dr. R. Zietse, internist-nefroloog.
2. http://www.vmszorg.nl/
3. http://www.vmszorg.nl/10-Themas/Nierinsufficientie
4. http://www.cbo.nl/Downloads/397/rl_jodium_2007.pdf
5. McCullough PA, Wolyn R, Rocher LL, Levin RN, O’Neill WW. Acute renal failure after coronary intervention: incidence, risk factors, and relationship to mortality. Am J Med 1997; 103: 368-75.
6. Hoste EA, De Waele JJ, Gevaert SA, Uchino S, Kellum JA. Sodium bicarbonate for prevention of contrast-induced acute kidney injury: a systematic review and meta-analysis. Nephrol Dial Transplant 2010; 25: 747-58.
7. Brar SS, Hiremath S, Dangas G, Mehran R, Brar SK, Leon MB. Sodium bicarbonate for the prevention of contrast induced-acute kidney injury: a systematic review and meta-analysis. Clin J Am Soc Nephrol 2009; 4: 1584-92.
8. Trivedi HS, Moore H, Nasr S, Aggarwal K, Agrawal A, Goel P, Hewett J. A randomized prospective trial to assess the role of saline hydration on the development of contrast nephrotoxicity. Nephron Clin Pract 2003; 93: C29-34.
9. Chen SL, Zhang J, Yei F, Zhu Z, Liu Z, Lin S, Chu J, Yan J, Zhang R, Kwan TW. Clinical outcomes of contrast-induced nephropathy in patients undergoing percutaneous coronary intervention: a prospective, multicenter, randomized study to analyze the effect of hydration and acetylcysteine. Int J Cardiol 2008; 126: 407-13.
Eerdere MC-artikelen over dit onderwerp: 'Gedeelde verantwoordelijkheid voor patiëntscreening?' Protocolleren van de verantwoordelijkheid voor het screenen van patiënten op contra-indicaties voor het gebruik van intraveneus contrastmiddel bij CT- en MRI-onderzoeken. Afstudeeropdracht HBO-MBRT Hanzehogeschool Groningen
<!--Indeling risicocategorie contrastnefropathie
VMS programma Preventie Contrastnefropathie: identificatie van hoogrisicopatiënten
hoog risico
eGFR <45 ml/min/1,73m2
eGFR <60 ml/min/1,73m2 en diabetes mellitus
eGFR <60 ml/min/1,73m2 en twee of meer andere risicofactoren*
M. Kahler of M. Waldenstrom met uitscheiding van lichte ketens in de urine
normaal risico
Alle situaties anders dan hoog risico
risicofactoren
perifeer vaatlijden
hartfalen
leeftijd >75 jaar
anemie (hematocriet <0,39 voor mannen en <0,36 voor vrouwen)
symptomatische hypotensie
contrastvolume >150 ml
verminderd effectief circulerend volume
diuretica en nefrotoxische geneesmiddelen (zoals NSAID’s)
Voorstel tot aanpassing definitie hoogrisicopatiënt
hoog risico
eGFR <30 ml/min/1,73m2
eGFR <45 ml/min/1,73m2 en diabetes mellitus
eGFR <45 ml/min/1,73m2 en twee of meer andere risicofactoren*
M. Kahler of M. Waldenstrom met uitscheiding van lichte ketens in de urine
normaal risico
Alle situaties anders dan hoog risico
risicofactoren
perifeer vaatlijden
hartfalen
leeftijd >75 jaar
anemie (hematocriet <0,39 voor mannen en <0,36 voor vrouwen)
symptomatische hypotensie
contrastvolume >150 ml
verminderd effectief circulerend volume
diuretica en nefrotoxische geneesmiddelen (zoals NSAID’s)
De nierfunctie (eGFR) wordt geschat middels de vier variabelen MDRD-formule, tenzij er bij de betreffende persoon sprake is van een acute nierinsufficiëntie, dan wel een voor de leeftijd en geslacht afwijkende spiermassa.3 Rood omkaderd de definitie van hoogrisicopatiënten zoals opgenomen in het VMS-programma.3 Groen omkaderd de door ons voorgestelde aangepaste definitie.-->


















W.F. Heesen
, Venlo
Ik wil graag bijval verlenen aan het stuk van collega Gansevoort met de oproep tot aanpassing van het programma preventie contrastnefropathie. Er is absoluut aandacht nodig voor de patienten met hoog risico op contrastnefropathie, om in principe verm...ijdbare schade te voorkomen. Anderzijds lijkt het vanuit de dagelijkse praktijk toch mogelijk wat overtrokken. Ook wij zien maar weinig patienten die echt door een contrastonderzoek dialyseafhankelijk worden, hoewel wij ons realiseren dat ook minder ernstig nierfunctieverlies vermeden dient te worden. MAar wij vragen ons af of er voldoende rekening wordt gehouden met veranderingen in de dagelijkse praktijk. Zo wordt bij een coronairangiografisch (CAG) onderzoek steeds minder vaak een linker ventrikelangiogram gemaakt, wat een aanzienlijke reductie van toegediend contrast tot gevolg heeft, vaak maar ca. 100 ml per patient. Dit terwijl hoog risico een toediening van 200 ml is. Daarentegen zien wij ook de nadelen van de huidige richtlijnen, met onder meer één risico wat nog niet door de auteurs als zodanig is genoemd: optreden van hartfalen door prehydratie. Ook bij aangepast hydratieschema (waarvoor dus inderdaad een opname ipv. een dagopname noodzakelijk is) zien wij toch met enige regelmaat benauwde patienten ten gevolge van overvulling door prehydratie bij het CAG onderzoek waardoor het onderzoek bemoeilijkt wordt of zelfs moet worden afgebroken. De nadelen: verlengde opname vanwege hartfalen, ook dan door diuretische behandeling risico nierschade, konden dan wel eens groter zijn dan de eventuele voordelen. Ik steun daarom de oproep tot herevaluatie van het programma, met de door de auteurs genoemde verlaging van de drempel qua klaring. De richtlijn zou dan ook best mogen worden uitgebreid met het vermijden van onnodig contrastbelastend onderzoek zoals het maken van een linker ventrikelangiogram bij een CAG. Expert-opinion based kan dat ook heel goed met een echocardiogram welke volstrekt onschadelijk is voor nieren en patient.
Wilfred Heesen, cardioloog
VieCuri Medisch Centrum voor Noord-Limburg